Baterai menjadi salah satu komponen yang paling sering dibutuhkan. Terlebih di era teknologi sekarang ini, hampir semua perangkat elektronik memerlukan komponen penting satu ini untuk kebutuhan daya dan dijadikan sebagai sumber listrik, mulai dari hp, laptop. Remote, senter, dan lainnya.
Dengan adanya komponen ini, maka Anda sudah tidak perlu lagi menyambungkan kabel listrik ketika akan mengaktifkan perangkat elektronik. Dengan begitu, perangkat elektronik bisa lebih praktis dan mudah untuk dibawa kemana-mana.
Apa yang Dimaksud dengan Baterai?
Baterai adalah kumpulan dari berbagai sel listrik yang dipakai untuk menyimpan energi kimia yang selanjutnya diubah ke energi listrik. Komponen utamanya terdiri atas dua bahan elektroda atau konduktor tak sejenis yang dicelup ke dalam larutan elektrolit atau penghantar listrik.
Salah satu elektroda ini bermuatan listrik positif dan lainnya bermuatan negatif. Pada ujung elektroda yang menonjol di atas elektrolit disebut dengan terminal positif dan terminal negatif.
Saat kedua terminal ini dihubungkan melalui kawat konduktor seperti tembaga, maka ars listrik akan mengalir lewat kawat dari terminal negatif menuju terminal positif. Untuk beda tekanan atau potensial listrik antar terminal tergantung dari bahan elektroda dan elektrolit, lalu diukur dalam Volt.
Untuk pemakaiannya, ada dua jenis baterai, yaitu ada yang bisa diisi ulang atau biasa disebut baterai sekunder dan ada yang tidak bisa diisi ulang atau biasa disebut baterai primer.
Fungsi Baterai
Baterai berfungsi sebagai penyedia atau penyuplai energi listrik untuk perangkat elektronik tanpa perlu tersambung ke listrik. Menurut sebuah penelitian, kita tidak bisa menangkap serta menyimpan listrik, tapi kita bisa menyimpan enerfi listrik ini dalam bentuk energi kimia memakai baterai.
Setelah itu, komponen ini akan mengubah energi kimia menjadi energi listrik kapan pun melalui proses elektrokimia. Energi listrik ini nantinya akan dipakai untuk menyalakan perangkat elektronik, seperti kamera, hp, radio, hingga mobil.
Jenis-Jenis Baterai
Komponen satu ini terdiri atas terminal positif (katoda) dan terminal negatif (anoda) serta elektrolit yang fungsinya sebagai penghantar. Output arus listrik yang dihasilkan yaitu arus DC (Direct Current) atau arus searah. Terdapat dua jenis baterai, yaitu sebagai berikut.
1. Baterai Primer atau Sekali Pakai (Single Use Battery)
Single use battery menjadi salah satu yang terpopuler di pasaran, bahkan hampir di setiap toko menjualnya. Hal ini dikarenakan pemakaiannya yang lebih luas serta harganya lebih terjangkau. Tegangannya sekitar 1,5 Volt dengan beragam jenis ukuran.
Ukuran yang paling umum yaitu AAA (ukuran terkecil), AA (ukuran kecil), C (ukuran medium), dan D (ukuran besar). Terdapat juga yang berbentuk kotak dan memiliki tegangan 6 Volt atau 9 Volt.
Ada beberapa jenis single use battery, diantaranya sebagai berikut.
a. Zinc Carbon
Nama lainnya yaitu “heavy duty” dan sering kali ditemui di berbagai toko maupun supermarket. Bahannya terbuat dari Zinc yang memiliki fungsi sebagai terminal negatif sekaligus sebagai pembungkus baterainya
Bahan lainnya yaitu Carbon yang berbentuk batang dan memiliki fungsi sebagai terminal positif. Jenis baterai zinc carbon termasuk yang relatif murah jika dibanding jenis yang lainnya.
b. Baterai Alkaline
Baterai jenis ini mempunyai daya tahan lebih lama namun harganya lebih mahal dibanding dengan jenis zinc carbon. Elektrolit yang dipakai yaitu Potassium hydroxide yang merupakan zat alkaline.
Alkaline saat ini banyak dipakai sebagai elektrolit, namun juga memakai bahan aktif lainnya yang digunakan sebagai elektroda.
c. Baterai Lithium
Jenis ini menjadi single use battery yang menawarkan kinerja lebih baik jika dibanding dengan yang lainnya. Penyimpanannya bisa lebih dari 10 tahun serta mampu bekerja di suhu yang sangat rendah.
Oleh karena itulah berbagai aplikasi memory backup pada jam tangan ataupun mikrokomputer sering menggunakannya. Bentuknya biasa dibuat mirip uang logam atau biasa diberi nama lain coin battery. Ada juga yang menyebutnya Button Cell karena mirip seperti kancing.
d. Silver Oxide
Jenis ini memiliki harga yang cukup mahal, karena harga perak (silver) yang cukup tinggi. Biasanya dipakai untuk menghasilkan energi yang tinggi, namun dengan bentuk yang cukup kecil serta ringan.
Bentuknya bisa menyerupai koin (coin battery) atau mirip kancing (button cell). Biasanya dipakai pada jam tangan, aplikasi militer, hingga kalkulator.
2. Baterai Sekunder atau Isi Ulang (Rechargeable)
Cara kerja baterai sekunder dalam menghasilkan arus listrik yaitu sama dengan primer. Namun, yang membesakan yaitu reaksi kimianya bisa berbalik (reversible). Ketika dipakai dengan menghubungkan beban di terminal baterai (discharge), maka elektron akan mengalir dari negatif menuju positif.
Sedangkan saat sumber energi luar (charger) dihubungkan, maka elektron akan mengalir dari positif menuju negatif, sehingga terjadi proses pengisian muatan. Contoh jenis baterai isi ulang diantaranya sebagai berikut.
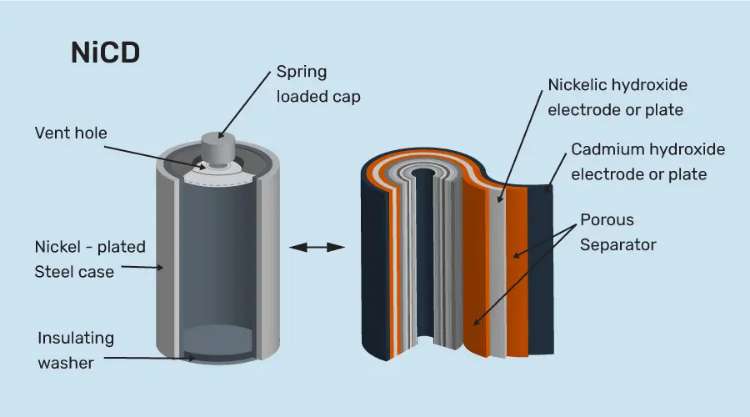
a. Nickel-Cadmium (Ni-Cd)
Jenis ini memakai Nickel Oxide Hydroxide dan Metallic Cadium yang dijadikan elektrolitnya. Selain itu juga bisa melakukan self-discharge sekitar 30% per bulan ketika tidak dipakai.
b. Nickel-Metal Hydride (Ni-MH)
Jenis ini mempunyai keunggulan mirip dengan Ni-Cd, namun jenis Ni-MH memiliki kapasitas 30% lebih besar dibanding dengan Ni-Cd.
Keunggulan lainnya yaitu bisa diisi ulang sampai ratusan kali, sehingga bisa menghemat biaya. Selain itu juga bisa melakukan self—discharge sekitar 40% per bulan saat tidak digunakan. Penggunaannya biasa dipakai untuk radio komunikasi dan juga kamera.
c. Baterai Lithium Ion (Li-Ion)
Jenis ini paling banyak dipakai pada perangkat ekejtronik portable, misalnya hp, kamera digital, dan laptop. Daya tahan siklusnya juga tinggi serta memiliki kapasitas lebih besar, yaitu 30% lebih tinggi dibanding Ni-MH.
Prinsip Kerjanya
Baterai mampu menghasilkan tegangan DC dengan cara mengubah energi kimia yang ada di dalamnya menjadi energi listrik melalui reaksi elektrokimia, reduksi – oksidasi (redoks). Terdapat dua jenis proses yang terjadi di dalamnya.
1. Proses Pengisian (Pengubahan Energi Listrik Menjadi Energi Kimia
Apabila dihubungkan dengan beban, maka kandungan elektronnya akan mengalir menuju elektroda positif (PbO2) dengan melewati beban dari elektroda negatif (Pb). Setelah itu, ion-ion negatif akan mengalir menuju elektroda positif dan ion-ion positif akan mengalir menuju elektroda negatif.
Arus listrik juga bisa mengalir yang disebabkan oleh adanya elektorn yang nantinya bergerak dari elektroda sel melalui reaksi ion antara molekul elektrolit dan molekul elektroda. Nantinya akan memberikan jalan bagi elektron untuk mengalir.
2. Proses Pengosongan (Proses Pengubahan Energi Kimia Menjadi Energi Listrik)
Proses ini menjadi kebalikan dari proses pengisian, yang mana proses pengosongan ini arus listrik dialirkan dengan arah berlawanan dengan arus listrik yang terjadi ketika proses pengisian. Dalam proses pengosongan ini, setiap molekul air akan terurai.
Ion oksigen bisa bebas bersatu dengan setiap atom Pb pada plat positif dan kemudian akan membentuk timah peroksida (PbO2).
Sementara untuk tiap pasang ion Hidrogen (2H+) yang dekat dengan plat negatif akan bersatu dengan ion negatif Sulfat (SO4-) pada plat negatif yang selanjutnya akan membentuk asam sulfat.
Baterai memang menjadi komponen praktis untuk mengaktifkan perangkat elektronik tanpa perlu menyambungkannya dengan kabel listrik. Fungsinya hampir dipakai untuk semua jenis perangkat elektronik protabel, mulai dari hp, senter, laptop, hingga remote.